
中国科学院上海有机化学研究所-生物医药快讯-2025-10
2025年10月FDA批准2种新药,具体如下:
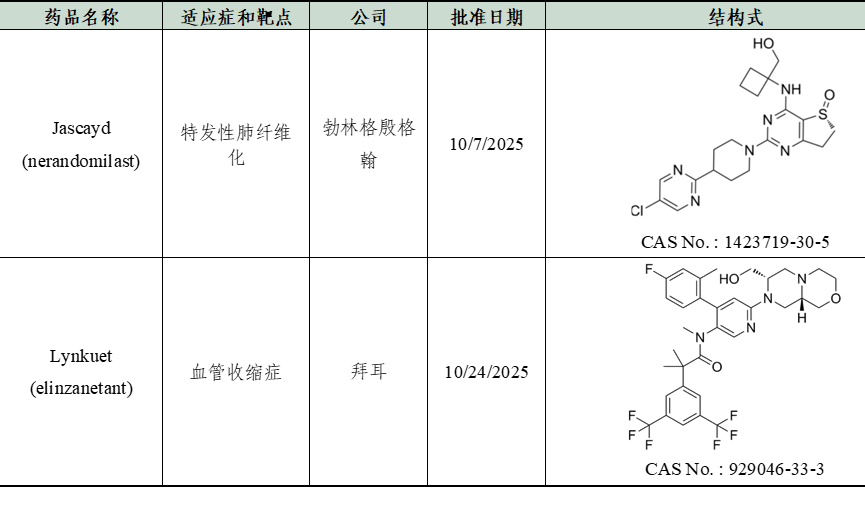
数据来源:Cortellis - Clarivate Analytics
结构式:
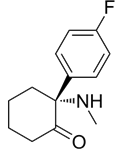
CAS No.:2881017-49-6
靶点/机制:N-甲基-D-天冬氨酸 (NMDA);
可能的适应症:重度抑郁;
公司/组织:Gilgamesh Pharmaceuticals;
结构式:
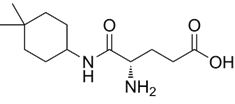
CAS No.:163000-63-3
靶点/机制:N-甲基-D-天冬氨酸 (NMDA) 受体调节剂;
可能的适应症:可卡因相关障碍;精神分裂症;
公司/组织:Rottapharm Madaus,Xytis;
结构式:
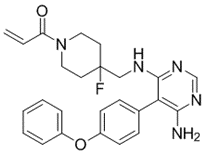
CAS No.:1415823-49-2
靶点/机制:布鲁顿氏酪氨酸激酶(BTK)抑制剂;
可能的适应症:B-细胞淋巴瘤;慢性淋巴细胞白血病;弥漫性大B-细胞淋巴瘤;
公司/组织:默克;
结构式:
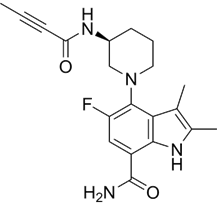
CAS No.:1912445-55-6
靶点/机制:布鲁顿氏酪氨酸激酶(BTK)抑制剂;
可能的适应症:特应性皮炎;类风湿性关节炎;干燥综合征;
公司/组织:百时美施贵宝;
结构式:
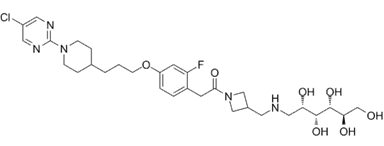
CAS No.:2639936-77-7
靶点/机制:Glucose-dependent insulinotropic receptor agonists 19(GPR119)激动剂;
可能的适应症:肥胖症; 二型糖尿病; 代谢病;
公司/组织:Kallyope;
结构式:
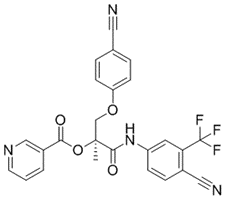
CAS No.:2442621-41-0
靶点/机制:SERT抑制剂;NET抑制剂;
可能的适应症:干眼症;乳腺癌;
公司/组织:宁波熙健医药,长春金赛药业;
结构式:
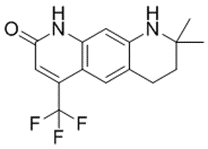
CAS No.:179897-43-9
靶点/机制:AR调节剂;
可能的适应症:髋骨折;
公司/组织:Ligand Pharmaceuticals;
结构式:
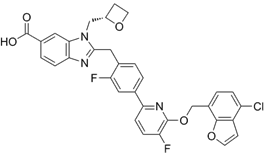
CAS No.:2969158-02-7
靶点/机制:GLP-1R 激动剂;
可能的适应症:肥胖症;
公司/组织:成都地奥制药;
结构式:
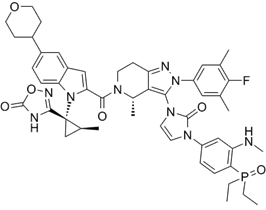
CAS No.:2685823-26-9
靶点/机制:GLP1R激动剂;
可能的适应症:Ⅱ型糖尿病; 肥胖症;
公司/组织:硕迪生物技术有限公司,Gasherbrum Bio;
结构式:
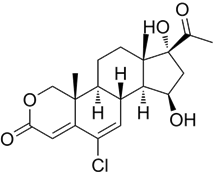
CAS No.:124548-08-9
靶点/机制:雄激素受体调节剂;
可能的适应症:前列腺增生;
公司/组织:Aska Pharmaceutical;
数据来源:Cortellis - Clarivate Analytics
结构式:
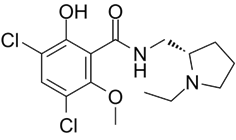
CAS No.:84225-95-6
靶点/机制:多巴胺D2/D3受体拮抗剂;
可能的适应症:注意力缺陷障碍伴多动;
公司/组织:阿斯利康;
终止(discontinued)时间:2000;
终止原因:未知
结构式:
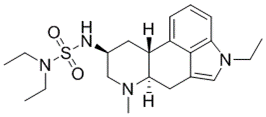
CAS No.:93822-42-5
靶点/机制:DRD2拮抗剂;
可能的适应症:帕金森症;
公司/组织:诺华;
终止(discontinued)时间:1991;
终止原因:毒性原因
结构式:
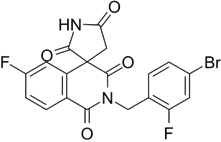
CAS No.:129688-50-2
靶点/机制:醛糖还原酶 (aldose reductase) 抑制剂;
可能的适应症:糖尿病;
公司/组织:辉瑞;
终止(discontinued)时间:2002/8;
终止原因:未知
结构式:
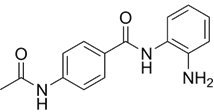
CAS No.:112522-64-2
靶点/机制:抗血管生成抑制剂;组蛋白去乙酰化酶抑制剂;
可能的适应症:乳腺癌;结直肠癌;肺癌; 胰腺癌;
公司/组织:辉瑞;
终止(discontinued)时间:2008/3;
终止原因:未知
结构式:
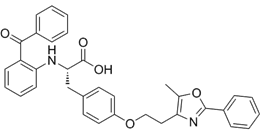
CAS No.:196808-45-4
靶点/机制:PPARγ激动剂;
可能的适应症:心衰;
公司/组织:GSK;
终止(discontinued)时间:2003;
终止原因:出现水肿迹象
信息来源:Cortellis - Clarivate Analytics
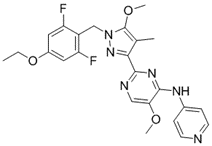
8d结构式:
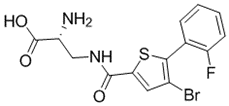
8j结构式:
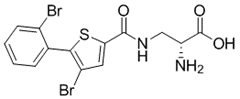
CAS No.:3092928-97-4
靶点/机制:GRIN2C/GluN1激动剂;
可能的适应症:神经系统疾病;
公司/组织:University of Copenhagen,山东大学;
最早出现preclinical data时间:2025/2;
来源文献:Fabao Zhao et al., J Med Chem, 2025, 68(3), 3572;
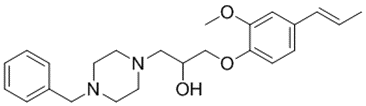
结构式:
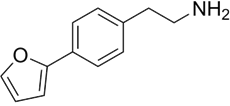
CAS No.:885466-70-6
靶点/机制:微量胺相关受体 1 (TAAR1)-Gq 激动剂;
可能的适应症:精神分裂;
公司/组织:山东大学;
最早出现preclinical data时间:2023/11;
来源文献:Shang P et al, Cell, 2023, 186(24), 5347.
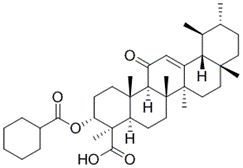
结构式:
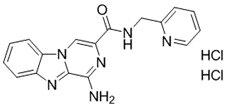
CAS No.:3031561-22-2
靶点/机制:AR/GR拮抗剂;
靶点/机制:腺苷A2A受体拮抗剂;
可能的适应症:肿瘤;
公司/组织:中山大学;
最早出现preclinical data时间:2022/6;
来源文献:Liu Shuhao et al., J Med Chem, 2022, 65(13), 8933.
结构式:
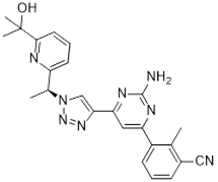
靶点/机制:腺苷A2A受体拮抗剂;
可能的适应症:肿瘤;
公司/组织:中山大学,长春中医药大学;
最早出现preclinical data时间:2025/6;
来源文献:Wang P et al., Eur J Pharmacol, 2025, 177535.
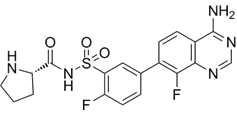
CAS No.:340304-55-4
靶点/机制:CRM1(染色体区域维持1)激动剂;
靶点/机制:细菌脯氨酰-tRNA 合成酶 (ProRS)抑制剂;
可能的适应症:细菌感染;
公司/组织:中山大学;
最早出现preclinical data时间:2025/4;
来源文献:Luo Z et al., Eur J Med Chem, 2025, 291, 117647.
结构式:
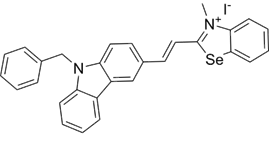
CAS No.:2829939-44-6
靶点/机制:c-MYC转录抑制剂;
可能的适应症:前列腺癌;
公司/组织:浙江大学;
最早出现preclinical data时间:2023/4;
来源文献:Wu TY et al., J Med Chem, 2023, 66(8), 5484.
结构式:
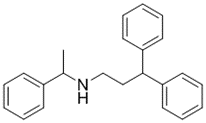
CAS No.:13042-18-7
靶点/机制:STING激动剂;
可能的适应症:肿瘤;
公司/组织:中山大学;
最早出现preclinical data时间:2024/1;
来源文献:Zhao M et al., Eur J Med Chem, 2024, 264, 116018.
结构式:
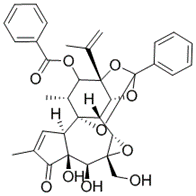
靶点/机制:KPNB1抑制剂;
可能的适应症:前列腺癌;
公司/组织:中山大学;
最早出现preclinical data时间:2022/9;
来源文献:Huang JL et al., J Am Chem Soc, 2022, 144, 17522.
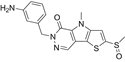
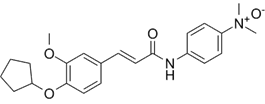
靶点/机制:脑源性神经营养因子 (BDNF)前药;
可能的适应症:神经退行性疾病;
公司/组织:中山大学;
最早出现preclinical data时间:2025/9;
来源文献:Zhang Z et al., Bioorg Med Chem Lett, 2025, 125-126, 130266.
结构式:
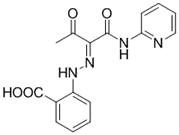
靶点/机制:RANK抑制剂;
可能的适应症:骨质疏松;
公司/组织:中山大学;
最早出现preclinical data时间:2022/9;
来源文献:Zhao C et al., Nature Comm, 2022, 13, 5338.
附件下载: