
中国科学院上海有机化学研究所-生物医药快讯-2025-04
2025年4月FDA批准2种新药,具体如下:
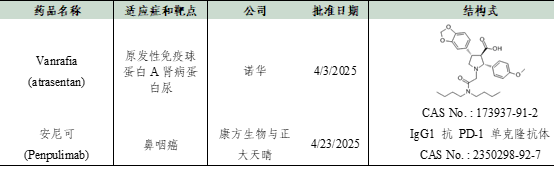
数据来源:Cortellis - Clarivate Analytics
结构式:
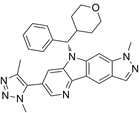
CAS No.:2115742-03-3
靶点/机制:BET 溴结构域抑制剂;
可能的适应症:鳞状细胞癌;
公司/组织:宁波文达医药;
结构式:
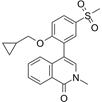
CAS No.:1706738-98-8
靶点/机制:BET 溴结构域抑制剂;
可能的适应症:胶质母细胞瘤;实体瘤;
公司/组织:百时美施贵宝,Quanticel Pharmaceuticals;
结构式:
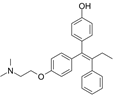
CAS No.:68392-35-8
靶点/机制:雌激素受体拮抗剂;选择性雌激素受体调节剂;
可能的适应症:乳腺癌;
公司/组织:Besins Healthcare,BHR Pharma;
结构式:
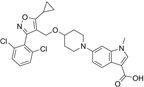
CAS No.:1103500-20-4
靶点/机制:FXR激动剂;
:非酒精性脂肪性肝炎;
公司/组织:礼来;
结构式:
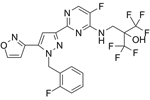
CAS No.:1628730-49-3
靶点/机制:可溶性鸟苷酸环化酶激动剂;
可能的适应症:心血管疾病;糖尿病肾病;
公司/组织:Akebia Therapeutics,Cyclerion Therapeutics,Ironwood Pharmaceuticals;
结构式:
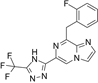
CAS No.:2201048-82-8
靶点/机制:可溶性鸟苷酸环化酶激动剂;
可能的适应症:阿尔兹海默症;MELAS 综合征;线粒体疾病;
公司/组织:Ironwood Pharmaceuticals,Cyclerion Therapeutics, Tisento Therapeutics;
结构式:
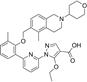
CAS No.:1579514-06-9
靶点/机制:可溶性鸟苷酸环化酶激动剂;
可能的适应症:糖尿病肾病;门静脉高压;肾衰竭;
公司/组织:勃林格殷格翰;
结构式:
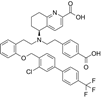
CAS No.:2231749-54-3
靶点/机制:鸟苷酸环化酶兴奋剂;
可能的适应症:心血管疾病;肾脏疾病;
公司/组织:拜耳;
结构式:
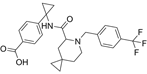
CAS No.:1417742-86-9
靶点/机制:EP4 受体拮抗剂;
可能的适应症:类风湿关节炎;
公司/组织:Rottapharm SpA;
结构式:
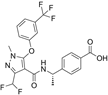
CAS No.:1369489-71-3
靶点/机制:前列腺素 E EP4 受体拮抗剂;
可能的适应症:直肠癌;
公司/组织:Adlai Nortye,Eisai;
数据来源:Cortellis - Clarivate Analytics
结构式:
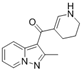
CAS No.:94457-09-7
靶点/机制:COXs抑制剂;
可能的适应症:血栓;
公司/组织:Kyorin Pharmaceutical;
终止(discontinued)时间:1995;
终止原因:未知
结构式:
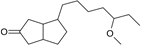
CAS No.:89672-11-7
靶点/机制:AR雄激素受体拮抗剂;
可能的适应症:痤疮;脱发;良性前列腺增生;
b-公司/组织:Cbd Pharmaceutical;
终止(discontinued)时间:2001;
终止原因:疗效不足
结构式:
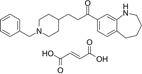
CAS No.:142852-51-5
靶点/机制:乙酰胆碱酯酶抑制剂;
可能的适应症:阿尔兹海默症;
公司/组织:Takeda;
终止(discontinued)时间:2003/1;
终止原因:缺乏剂量依赖效应
结构式:
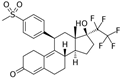
CAS No.:1262108-14-4
靶点/机制:孕酮受体拮抗剂;
可能的适应症:子宫内膜异位症;子宫肌瘤;
公司/组织:拜尔;
终止(discontinued)时间:2022/6;
终止原因:长期毒理研究中存在安全问题
结构式:
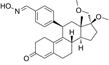
CAS No.:199396-76-4
靶点/机制:孕激素受体调节剂;
可能的适应症:子宫内膜异位症;更年期综合征;子宫肌瘤;
公司/组织:EnTec ,TAP Pharmaceutical;
终止(discontinued)时间:2009/2;
终止原因:未知
信息来源:Cortellis - Clarivate Analytics
结构式:
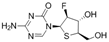
CAS No.:2414069-54-6
靶点/机制:DNMT1抑制剂;
可能的适应症:肿瘤;
公司/组织:美国国立癌症研究所;
最早出现preclinical data时间:2021/6;
来源文献:Joel Morris et al., Mol Cancer Ther, 2021, 20, 625.
结构式:
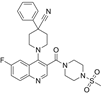
CAS No.:2231079-74-4
靶点/机制:乙醛脱氢酶 (aldehyde dehydrogenase (ALDH1A1)) 抑制剂;
可能的适应症:T细胞白血病;
公司/组织:加利福尼亚大学;
最早出现preclinical data时间:2018/6;
来源文献:Yang SM et al, J Med Chem, 2018, 61, 4883.
结构式:
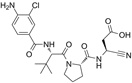
CAS No.:1230628-71-3
靶点/机制:caspase 1抑制剂;
可能的适应症:星型细胞瘤;
公司/组织:National Institute of Diabetes & Digestive & Kidney Diseases;
最早出现preclinical data时间:2017/9;
来源文献:Adriaenssens Y et al., Org Biomol Chem, 2017, 15(35), 7456.
结构式:
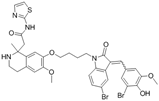
CAS No.:2974496-96-1
靶点/机制:PCSK9降解剂;
可能的适应症:动脉粥样硬化;
公司/组织:复旦大学;
最早出现preclinical data时间:2024/5;
来源文献:Zhirong Ouyang et al., J Med Chem, 2023, 67, 433.
结构式:
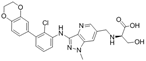
CAS No.:2761306-51-6
靶点/机制:PD-1&PDL1抑制剂;
可能的适应症:肿瘤;
公司/组织:中国医学科学院药物研究所;
最早出现preclinical data时间:2021/9;
来源文献:Momar Ndao et al., Bioorg Chem, 2021, 114, 105034.
结构式:
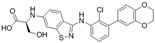
CAS No.:184582-62-5
靶点/机制:PD-1&PDL1抑制剂;
可能的适应症:肿瘤;
公司/组织:中国医学科学院药物研究所;
最早出现preclinical data时间:2021/5;
来源文献:Hao Chen et al., Eur J Med Chem, 2021, 217, 113377.
结构式:
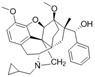
CAS No.:2765571-51-3
靶点/机制:κ阿片受体激动剂;
可能的适应症:镇痛;
公司/组织:复旦大学;
最早出现preclinical data时间:2022/7;
来源文献:Linghui Kong et al., J Med Chem, 2022, 65, 10377.
结构式:
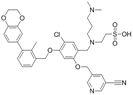
CAS No.:2566710-63-0
靶点/机制:PD-1&PDL1抑制剂;
可能的适应症:肿瘤;
公司/组织:复旦大学;
最早出现preclinical data时间:2021/7;
来源文献:Chenglong Liu et al., Br J Pharmacol, 2021, 178, 2651.
结构式:
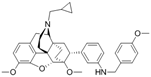
CAS No.:2640604-73-3
靶点/机制:κ阿片受体激动剂;
可能的适应症:镇痛;
公司/组织:复旦大学;
最早出现preclinical data时间:2021/8;
来源文献:Qian He et al., J Med Chem, 2021, 64, 12413.
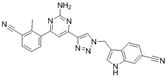
靶点/机制:A2AR/A2BR拮抗剂;
可能的适应症:肿瘤;
公司/组织:复旦大学;
最早出现preclinical data时间:2024/3;
来源文献:Haojie Wang et al., J Med Chem, 2024, 67, 5075.
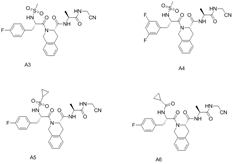
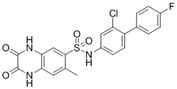
附件下载: