
中国科学院上海有机化学研究所-生物医药快讯-2024-02
2024年2月FDA批准1种新药,具体如下:
表 2024年FDA批准新药(2月)
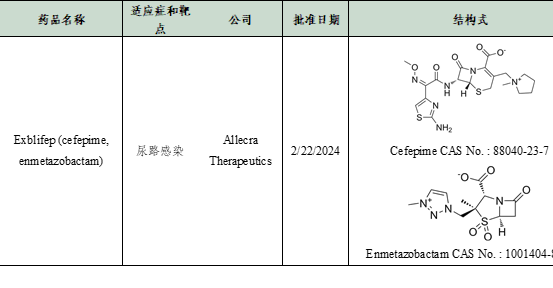
数据来源:Cortellis - Clarivate Analytics
结构式:
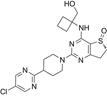
CAS No.:1423719-30-5
靶点/机制:4 型环核苷酸磷酸二酯酶抑制剂;
可能的适应症:特发性肺纤维化;间质性肺病;
公司/组织:勃林格殷格翰;
结构式:
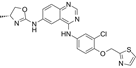
CAS No.:845272-21-1
靶点/机制:表皮生长因子受体拮抗剂;ERBB 2/4受体拮抗剂;
可能的适应症:胆道癌;胃癌;
公司/组织:Array BioPharma,ASLAN Pharmaceuticals;
结构式:
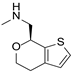
CAS No.:266359-83-5
靶点/机制:5-HT1A 血清素受体激动剂;痕量胺相关受体 1 激动剂;
可能的适应症:重度抑郁症;精神分裂症;广泛性焦虑症;
公司/组织:Dainippon Sumitomo Pharma,Sumitomo Pharma;
结构式:

CAS No.:104632-28-2
靶点/机制:抗氧化剂;细胞凋亡抑制剂;多巴胺受体激动剂;
可能的适应症:哮喘;
公司/组织:University of Virginia,Areteia Therapeutics,Biogen Idec,Knopp Biosciences;
结构式:
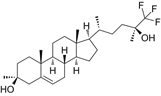
CAS No.:1629853-48-0
靶点/机制:NMDA 受体调节剂;
可能的适应症:亨廷顿舞蹈症;
公司/组织:SAGE Therapeutics;
结构式:
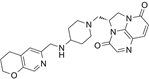
CAS No.:1075236-89-3
靶点/机制:三氮杂苊烯细菌II型拓扑异构酶抑制剂;
可能的适应症:淋病;尿路感染;
公司/组织:GSK,INSERM;
结构式:
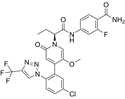
CAS No.:2064121-65-7
靶点/机制:凝血因子 FXIa 抑制剂;
可能的适应症:心房颤动;中风;血栓栓塞症;
公司/组织:拜尔;
结构式:

CAS No.:2170729-29-8
靶点/机制:醛还原酶抑制剂;
可能的适应症:中枢神经系统疾病;
公司/组织:Applied Therapeutics
结构式:
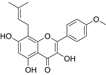
CAS No.:118525-40-9
靶点/机制:雌激素受体α调节剂;
可能的适应症:肝癌;
公司/组织:Shenogen Pharma;
结构式:
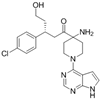
CAS No.:1143532-39-1
靶点/机制:原癌基因蛋白 c-akt 抑制剂;
可能的适应症:前列腺癌;三阴性乳腺癌;
公司/组织:Astex Therapeutics,阿斯利康;
数据来源:Cortellis - Clarivate Analytics
结构式:
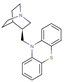
CAS No.:88598-74-7
靶点/机制:组胺 H1受体拮抗剂;毒蕈碱受体拮抗剂;
可能的适应症:过敏性鼻炎;
公司/组织:Pierre Fabre;
终止(discontinued)时间:2021/8;
终止原因:未知
结构式:
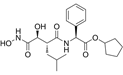
CAS No.:238750-77-1
靶点/机制:氨基肽酶抑制剂;
可能的适应症:急性髓性白血病;骨髓增生异常综合征;前体细胞淋巴细胞白血病;
公司/组织:Vernalis,Cardiff University,CTI BioPharma;
终止(discontinued)时间:2020;
终止原因:毒性
结构式:
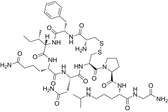
CAS No.:876296-47-8
靶点/机制:加压素 V1A 受体激动剂;
可能的适应症:败血性休克;
公司/组织:Ferring Pharmaceuticals;
终止(discontinued)时间:2021/3;
终止原因:未知
结构式:
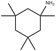
CAS No.:219810-59-0
靶点/机制:烟碱受体拮抗剂;NMDA 受体拮抗剂;
可能的适应症:酗酒;老年痴呆症;
公司/组织:Forest Laboratories,Kyorin Pharmaceutical,Merz Pharma;
终止(discontinued)时间:2019/7;
终止原因:未知
结构式:

CAS No.:936622-80-9
靶点/机制:细胞膜调节剂;细胞壁抑制剂;
可能的适应症:葡萄球菌感染;
公司/组织:Helperby Therapeutics;
终止(discontinued)时间:2019/8;
终止原因:疗效不足
信息来源:Cortellis - Clarivate Analytics
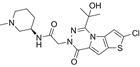
CAS No.:2409825-32-5
靶点/机制:NOD 样受体热蛋白结构域蛋白3(NLRP3)抑制剂;
可能的适应症:腹膜炎;
公司/组织:诺华;
最早出现preclinical data时间:2024/1;
来源文献:Juraj Velcicky et al., J Med Chem, 2024, 67(2), 1544.
结构式:
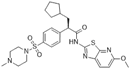
CAS No.:866772-52-3
靶点/机制:葡萄糖激酶激活剂;
可能的适应症:糖尿病;
公司/组织:诺华;
最早出现preclinical data时间:2009/10;
来源文献:Gregory R Bebernitz, 36th American Chemical Society Northeast Regional Meeting, 2009.
结构式:
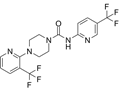
CAS No.:821768-06-3
靶点/机制:TRPM8 蛋白抑制剂;TRPV1 受体拮抗剂;
可能的适应症:咳嗽;
公司/组织:强生;
最早出现preclinical data时间:2014/4;
来源文献:Xingjuan Chen et al., J Biol Chem, 2014, 289(14), 9600.
结构式:
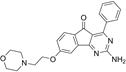
CAS No.:1147271-25-7
靶点/机制:腺苷 A2A/A1 拮抗剂;
可能的适应症:帕金森症;
公司/组织:强生;
最早出现preclinical data时间:2005/1;
来源文献:John R. Atack et al., ACS Chem Neurosci, 2014, 5, 1005.
结构式:
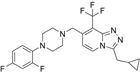
CAS No.:1254979-66-2
靶点/机制:代谢型谷氨酸受体 2 的正异构调节剂;
可能的适应症:阿尔兹海默症;
公司/组织:中国药科大学;
最早出现preclinical data时间:2021/5;
来源文献:Cid JM et al., J Med Chem, 2016, 59(18), 8495.
结构式:
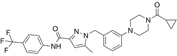
CAS No.:2798953-78-1
靶点/机制:线粒体复合物 I(CI)抑制剂;
可能的适应症:肿瘤;
公司/组织:四川大学;
最早出现preclinical data时间:2023/10;
来源文献:Zhou Yang et al., Eur J Med Chem, 2023, 258, 115576.
结构式:
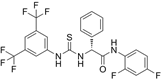
CAS No.:2101517-69-3
靶点/机制:unc-51 类自噬激活激酶 1(ULK1)激活剂;
可能的适应症:帕金森症;
公司/组织:四川大学;
最早出现preclinical data时间:2018/4;
来源文献:Ouyang L et al., J Med Chem, 2018, 61(7), 2776.
结构式:
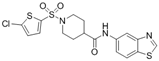
CAS No.:941924-87-4
靶点/机制:毒蕈碱乙酰胆碱受体亚型 5(M5)拮抗剂;
可能的适应症:药物滥用症;抑郁症;焦虑症;
公司/组织:Vanderbilt University;
最早出现preclinical data时间:2022/11;
来源文献:Everaerts W et al., Bioorg Med Chem Lett, 2022, 76, 128988.
结构式:
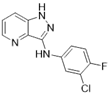
CAS No.:1330624-42-4
靶点/机制:mGluR4正向变构调节剂;
可能的适应症:帕金森症;
公司/组织:Vanderbilt University;
最早出现preclinical data时间:2023/7;
来源文献:Niswender CM et al., ACS Chem Neurosci, 2016, 7 (9), 1201.
结构式:
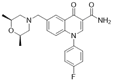
CAS No.:1821325-29-4
靶点/机制:mGluR2拮抗剂;
可能的适应症:中枢神经系统疾病;
公司/组织:Vanderbilt University;
最早出现preclinical data时间:2015/11;
来源文献:Felts AS et al., J Med Chem, 2015, 58(22), 9027.
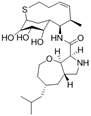
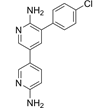 CAS No. :1431985-92-0
CAS No. :1431985-92-0
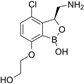
 CAS No. : 1811510-56-1
CAS No. : 1811510-56-1
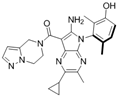
 CAS No. : 2131798-12-2
CAS No. : 2131798-12-2
附件下载: