
中国科学院上海有机化学研究所-生物医药快讯-2024-05
2024年5月FDA批准1种新药,具体如下:

数据来源:Cortellis - Clarivate Analytics
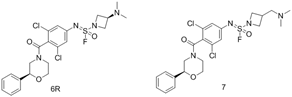
结构式:
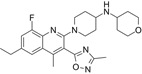
CAS No.:2244614-14-8
靶点/机制:阿片 kappa 受体拮抗剂;
可能的适应症:重度抑郁症;
公司/组织:BlackThorn Therapeutics,Neumora Therapeutics;
结构式:
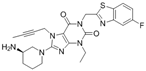
CAS No.:1518906-09-6
靶点/机制:二肽基肽酶 4 抑制剂;
可能的适应症:Ⅱ型糖尿病;
公司/组织:Easton Biopharmaceuticals;
结构式:
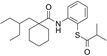
CAS No.:211513-37-0
靶点/机制:胆固醇酯转移蛋白抑制剂;
可能的适应症:急性冠状动脉综合征;
公司/组织:Japan Tobacco,罗氏;
结构式:
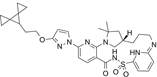
CAS No.:2374124-49-7
靶点/机制:囊性纤维化跨膜传导调节器调节剂;
可能的适应症:囊性纤维化;
公司/组织:Vertex Pharmaceuticals;
结构式:
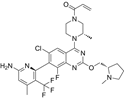
CAS No.:2417987-45-0
靶点/机制:KRAS 蛋白抑制剂;
可能的适应症:非小细胞肺癌;
公司/组织:基因泰克,罗氏;
结构式:
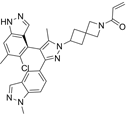
CAS No.:2653994-08-0
靶点/机制:KRAS 蛋白抑制剂;
可能的适应症:非小细胞肺癌;
公司/组织:诺华;
结构式:
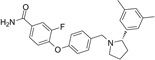
CAS No.:1174130-61-0
靶点/机制:阿尔兹海默症tau PET影像诊断剂;
可能的适应症:阿尔茨海默病;痴呆症;
公司/组织:礼来,强生,洛克菲勒大学;
结构式:
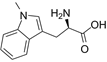
CAS No.:110117-83-4
靶点/机制:吲哚胺-吡咯-2,3-二氧化酶抑制剂;
可能的适应症:恶性黑色素瘤;
公司/组织:Lankenau Institute for Medical Research;
结构式:
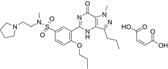
CAS No.:1422955-52-9
靶点/机制:5 型磷酸二酯酶 (PDE5) 抑制剂;
可能的适应症:勃起功能障碍;
公司/组织:上海特化医药;
结构式:
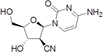
CAS No.:135598-68-4
靶点/机制:急性髓性白血病;
可能的适应症:DNA 定向 DNA 聚合酶抑制剂;
公司/组织:Delta-Fly Pharma,Nippon Shinyaku;
数据来源:Cortellis - Clarivate Analytics
结构式:
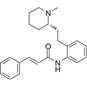
CAS No.:58754-46-4
靶点/机制:羟色胺 2A 受体拮抗剂;
可能的适应症:痔疮;
公司/组织:Sam Amer,Ventrus Biosciences;
终止(discontinued)时间:2012/6;
终止原因:没有达到预期疗效
结构式:
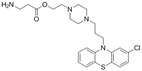
CAS No.:503537-33-5
靶点/机制:多巴胺受体拮抗剂;GABA 受体激动剂;
可能的适应症:精神分裂症;
公司/组织:Bar-Ilan University,Tel Aviv University,BioLineRx;
终止(discontinued)时间:2013/3;
终止原因:中期试验未达到实验终点
结构式:
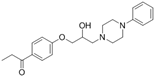
CAS No.:34675-77-9
靶点/机制:羟色胺摄取抑制剂;
可能的适应症:重度抑郁;
公司/组织:Central Drug Research Institute;
终止(discontinued)时间:2013/11;
终止原因:未知
结构式:
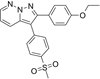
CAS No.:221148-46-5
靶点/机制:环氧合酶 -2 (COX-2) 抑制剂;
可能的适应症:骨关节炎;疼痛;类风湿性关节炎;
公司/组织:GSK;
终止(discontinued)时间:2004/11;
终止原因:未知
结构式:
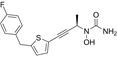
CAS No.:154355-76-7
靶点/机制:5-脂加氧酶 (5-LO) 抑制剂;
可能的适应症:哮喘;
公司/组织:Abbott,VIA Pharmaceuticals;
终止(discontinued)时间:2013/1;
终止原因:疗效不足
信息来源:Cortellis - Clarivate Analytics
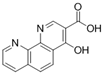
CAS No.:2952994-34-0
靶点/机制:低氧诱导因子1α稳定剂;
可能的适应症:帕金森症;
公司/组织:University of Southern Denmark;
最早出现preclinical data时间:2009/1;
来源文献:Kenneth Thirstrup et al., J Neurosci Res, 2009, 7(87), 1686.
结构式:
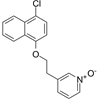
CAS No.:2487253-25-6
靶点/机制:G蛋白受体偏向性GPR84激动剂;
可能的适应症:癌症;
公司/组织:University of Oxford;
最早出现preclinical data时间:2019/9;
来源文献:Lucy D et al., ACS Chem Biol, 2019, 14(9), 2055.
OX-04528 结构式:
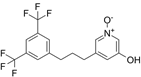
OX-04529 结构式:
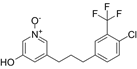
靶点/机制:G蛋白受体偏向性GPR84激动剂;
可能的适应症:肿瘤;
公司/组织:University of Oxford;
最早出现preclinical data时间:2023/12;
来源文献:Wang P et al., J Med Chem, 2024, 67(1), 110.
结构式:
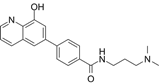
CAS No.: 1222800-79-4
靶点/机制:jumonji histone demethylase (JMJD2)抑制剂;KDM1A (赖氨酸特异性组蛋白脱甲基酶-1)抑制剂;
可能的适应症:疱疹病毒 (HSV) 和人巨细胞病毒 (hCMV) 感染;
公司/组织:University of Oxford;
最早出现preclinical data时间:2012/12;
来源文献:Ganesha Rai et al., Probe Reports from the NIH Molecular Libraries Program, 2012.
结构式:

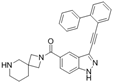
靶点/机制:结核分枝杆菌 (Mtb) 23S 细菌核糖体抑制剂;
可能的适应症:结核;
公司/组织:Sanofi;
最早出现preclinical data时间:2023/3;
来源文献:Yusupova, Gulnara et al., Cell, 2023, 5(186), 1013.
结构式:
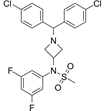
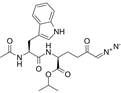
CAS No.:358970-97-5
靶点/机制:大麻素受体 CB1 拮抗剂;
可能的适应症:恶心和呕吐;
公司/组织:Sanofi;
最早出现preclinical data时间:2007/9;
来源文献:Andreas W Herling et al., Am J Physiol Endocrinol Metab, 2007, 293, E826.
结构式:
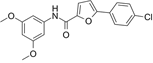
CAS No.:944261-79-4
靶点/机制:Nav1.8 钠通道阻断剂;
可能的适应症:炎症性疼痛;
公司/组织:Abbott;
最早出现preclinical data时间:2007/3;
来源文献:Jarvis MF et al., PANS, 2007, 104(20), 8520.
结构式:
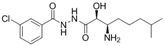
CAS No.:369358-07-6
靶点/机制:氨基肽酶抑制剂;
可能的适应症:超敏反应;哮喘;
公司/组织:Abbott;
最早出现preclinical data时间:2006/4;
来源文献:George S. Sheppard et al., Bioorg Med Chem Lett, 2004, 14, 865.
结构式:
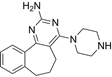
CAS No.:1027330-82-0
靶点/机制:组胺H4 受体的拮抗剂;
可能的适应症:炎性疾病;
公司/组织:Abbott;
最早出现preclinical data时间:2009/5;
来源文献:M I Strakhova et al., Br J Pharmacol, 2009, 157, 44.
结构式:
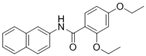
CAS No.:415695-10-2
靶点/机制:BK channel激动剂;
可能的适应症:抽搐;
公司/组织:Abbott;
最早出现preclinical data时间:2007/1;
来源文献:C C Shieh et al., Br J Pharmacol, 2007, 151, 798.
信息编辑:图书馆&科研管理处
意见反馈及建议,请联系:
邱婷45614 qiuting@sioc.ac.cn
数据来源:drughunter.com

2024 年 4 月的 “本月分子 ”榜单如下:
1. IAG933 - 诺华公司推出的一种强效、选择性的一流抑制剂,可直接抑制 YAP/TAZ 与 TEAD 之间的蛋白相互作用 (PPI)。通过阻断这种 PPI,IAG933 可干扰 Hippo 信号通路下游的致癌功能,尤其是在间皮瘤和其他 NF2 功能缺失突变或 YAP/TAZ 融合的肿瘤中。这种抑制可降低转录活性,诱导癌细胞死亡,从而使异种移植模型中的肿瘤明显缩小。此外,临床前将 IAG933 与其他靶向疗法(即 RTK、KRAS 突变选择性抑制剂和 MAPK 抑制剂)相结合,有望提高疗效和治疗反应的持久性。目前,IAG933 正在一项针对Hippo 通路改变的实体瘤的临床Ⅰ期试验。
2. HRO761 - 诺华公司发现的一种强效、选择性 WRN 螺旋酶抑制剂,靶向 MSI(微卫星不稳定性)癌细胞。HRO761 是通过一种新颖的靶点发现和先导优化方法确定的,它能在 D1 和 D2 螺旋酶结构域的界面上与 WRN 异源结合,将其锁定在非活性构象中。在体内,HRO761 在 MSI 和患者衍生异种移植模型中表现出剂量依赖性 DNA 损伤和肿瘤抑制作用。目前正在进行其对 MSI 大肠癌和其他 MSI 高的实体瘤患者的安全性和有效性的临床Ⅰ期试验(NCT05838768)。
3. RMC-6236- Revolution Medicine 的口服非共价三复合分子胶,可诱导无处不在的细胞内伴侣 CypA(cyclophilin A)与 GTP 结合(ON)状态的 RAS 之间的复合物,有效抑制 WT 和多种 RAS(ON)异构体,包括 G12V/A、G13X 和 Q61X 等 “不可药用 ”突变体。在小鼠临床前异种移植模型中,RMC-6236 的口服耐受性良好,并能显著抑制肿瘤生长。正在进行的一项临床I/Ib 试验(NCT05379985)的初步临床结果表明,两名晚期 KRAS G12X 肺腺癌和胰腺腺癌患者在每天服用 300 毫克的剂量后,客观反应良好。最前沿的临床试验是 RMC-6236 与标准治疗相结合的临床I/II (NCT06162221) 研究。
4. Tavapadon - 一种潜在的治疗帕金森病的 D1/D5 多巴胺受体第一类选择性部分激动剂,可直接影响运动活动,同时最大限度地减少非选择性刺激多巴胺药物的典型副作用。今年 4 月,Cerevel 公司分享了其 TEMPO-3 III 期试验(NCT04542499)的初步结果,该试验评估了 tavapadon 作为左旋多巴辅助疗法治疗帕金森病的效果。该试验达到了主要终点,与安慰剂相比,27 周内无运动障碍的总 “开机 ”时间有统计学意义的显著增加(1.7 小时对 0.6 小时)。12 月,艾伯维斥资 87 亿美元收购了 Cerevel 公司,tavapadon 成为艾伯维产品线的一部分。
5. KT-333 - Kymera Therapeutics公司生产的一种高选择性、基于VHL的STAT3异功能降解剂。STAT3是一种参与各种细胞因子和生长因子信号通路的转录因子。在依赖STAT3的癌症中,STAT3 的过度激活会促进免疫抑制、肿瘤进展和转移。这种首次进入临床的转录因子降解剂已在人体中显示出靶向 STAT3 蛋白降解和通路抑制的证据,以及抗肿瘤活性的早期迹象。KT-333 正在复发或难治性淋巴瘤、白血病和实体瘤患者的临床I期 试验(NCT05225584)中进行评估。
6. TNG908 - 来自 Tango Therapeutics 的一种口服 MTA 合作型血脑屏障渗透 PRMT5 抑制剂。TNG908在MTAP缺失异种移植和皮下多形性胶质母细胞瘤 (GBM) 模型中都能引起肿瘤的深度消退,并且具有高渗透性,在 MDCK-MDR1 和 BCRP 试验中无主要的流出责任。Tango的另一种PRMT5抑制剂TNG462与TNG908具有互补性,对PRMT5:MTA复合物的效力和选择性明显高于PRMT5,但缺乏中枢神经系统暴露。一项 I/II 期研究(NCT05275478)正在评估 TNG908 在同基因 MTAP 缺失癌症(包括 GBM)中的应用。
7. NST-628 - Nested Therapeutics 的强效口服(pan-RAF)-MEK 分子胶,通过阻断 BRAF-CRAF 异源二聚体的形成来抑制 MEK 的磷酸化和活化,为抑制 RAS-MAPK 信号通路提供了一种独特的机制。这种方法能阻断 BRAF-CRAF 异二聚体的形成,而这正是目前 RAF 抑制剂的一个共同局限。NST-628 具有血脑屏障穿透性,在细胞系和患者衍生肿瘤模型(包括具有不同 MAPK 通路突变的颅内模型)中显示出广泛的疗效。NST-628 正在一项临床I 期试验(NCT06326411)中接受评估,该试验针对的是已用尽标准治疗方案的 MAPK 通路突变/依赖性晚期实体瘤成年患者。
8. CVN293 - 来自 Cerevance 的 KCNK13 强效、选择性和脑穿透抑制剂。KCNK13 是一种 K+ 离子通道,在小胶质细胞中具有高度特异性表达,参与 NLRP3 炎性体的典型激活,导致神经炎症,并在各种神经退行性疾病中上调。研究表明,CVN293 可通过抑制 LPS 刺激的小鼠小胶质细胞中的 NLRP3 炎性体减少 IL-1β的产生,目前正在进行一项临床I期试验,以研究其在健康受试者中的安全性、耐受性和PK。
9. BDTX-1535 - 由 Black Diamond Therapeutics 发现的第四代脑穿透性 TKI,可靶向 NSCLC 中的多种致癌表皮生长因子受体突变,包括经典和非经典驱动突变以及C797S 抗性突变。临床前研究表明,这种“MasterKey”抑制剂可抑制 50多种不同的致癌表皮生长因子受体突变。此外,BDTX-1535 还能抑制 GBM 中常见的表皮生长因子受体胞外结构域突变,避免了早期可逆 TKIs 常常出现的矛盾性激活。目前正在进行的临床试验(NCT06072586 和 NCT05256290)评估其对GBM和NSCLC患者的疗效。
10. sovleplenib - 和记黄埔医药通过优化吡啶并[3,4-b]吡嗪支架发现的一种强效、选择性 Syk 抑制剂。这种小分子具有良好的临床前PK特征,在胶原诱导的关节炎模型中显示出强大的抗炎功效。索夫来普奈目前正在进行一项临床III期试验(NCT05029635),以确定其治疗慢性免疫性血小板减少性紫癜的安全性和有效性。
附件下载: